
Etyl benzen hay Ethylbenzen là một hợp chất hữu cơ có công thứ phân tử là C8H10. Phần lớn lượng Ethylbenzen được sản xuất ứng dụng trong điều chế styrene. Ngoài ra hóa chất này còn được ứng dụng trong điều chế một số hóa chất khác hay làm dung môi trong mực, làm sơn dầu, chất kết dính cao su. Cùng tìm hiểu thêm những thông tin thú vị khác về etylbenzen ngay dưới đây
1. Etyl benzen là gì
Etylbenzen là một hợp chất có thuộc tính tương đồng với ankan và có nhiều ứng dụng quan trọng trong lĩnh vực hóa học. Được xem như một tạp chất của benzen, etylbenzen có khả năng tham gia vào nhiều quy trình sản xuất quan trọng. Mặc dù etylbenzen được biết đến là một tác nhân có khả năng gây hại cho sức khỏe trong môi trường làm việc, nhưng thông qua việc tuân thủ các biện pháp an toàn và sử dụng đúng cách, chúng ta có thể tận dụng những lợi ích mà nó mang lại mà không gây hại cho sức khỏe con người.
2. Tính chất lý hóa của Etyl benzen
2.1. Tính chất vật lý
Etylbenzen là một dạng đồng đẳng của benzen, có công thức C8H10. Nó là một chất lỏng không màu, có mùi thơm và ít tan trong nước.
Trọng lượng phân tử: 106,16 g/mol
Mật độ: 0,864 g / mL
Điểm sôi: 138,5 °C
Điểm nóng chảy: −47,4 °C
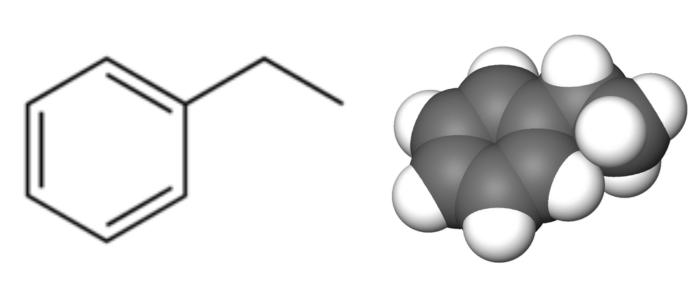
Hình: Công thức cấu tạo của Etyl Benzen
2.2. Tính chất hóa học
Etylbenzen có tính chất tương tự với benzen và các hiđrocacbon no khác. Cụ thể, nó thể hiện tính chất hóa học tương đồng với ankan, bao gồm khả năng tham gia vào các phản ứng gắn phân tử hidro và phản ứng gắn phân tử oxi.
Hơn nữa, etylbenzen cũng mang tính chất độc hại. Nó đã được xác định là một tác nhân có khả năng gây bệnh nghề nghiệp, có thể gây ra vấn đề về sức khỏe khi tiếp xúc kéo dài và lặp đi lặp lại. Thêm vào đó, khả năng gây cháy nổ của etylbenzen đặt ra yêu cầu cẩn trọng trong việc sử dụng, và việc tuân thủ các biện pháp an toàn khi sử dụng
Một số phản ứng hóa học nổi bật của Etyl Benzen
Phản ứng etylbenzen + kmno4
7C8H10 + 18KMnO4 → 8C7H5O2K + 18MnO2 + 10KOH + 10H2O
Phản ứng etylbenzen + h2
7C8H10 + 21H2 → 8C7H14
Phản ứng etylbenzen + hno3
C8H10 + HNO3 → C6H3CH3CH3NO2 + H2O
Phản ứng etylbenzen + cl2
C8H10 + Cl2 → C8H9Cl + HCl
3. Điều chế Etyl benzen
Trong công nghiệp, etylbenzen được điều chế thông qua phản ứng alkylation bằng cách kết hợp benzen và etilen dưới sự tác động của xúc tác acid như AlCl3. Xúc tác này giúp tạo ra etylbenzen thông qua việc gắn nhóm etyl vào vòng benzen. Sau đó, sản phẩm được tách ra và xử lý để thu được etylbenzen tinh khiết.
4. Ứng dụng của Etylbenzen
Etylbenzen có nhiều ứng dụng quan trọng trong ngành hóa học và công nghiệp:
- Sản xuất styren: Etylbenzen là nguyên liệu quan trọng trong việc sản xuất styren, một hợp chất được sử dụng rộng rãi để sản xuất nhựa polystyren, cao su styren-butadien (SBR) và các sản phẩm khác.
- Sản xuất polystyren: Styren được sản xuất từ etylbenzen là thành phần cơ bản để sản xuất polystyren, một loại nhựa cứng, trong suốt và dễ gia công. Polystyren được sử dụng trong các sản phẩm như hộp đựng thực phẩm, bộ đồ chơi, vỏ điện thoại và nhiều ứng dụng khác.
- Sản xuất hóa chất tổng hợp: Etylbenzen là nguyên liệu trong việc sản xuất các hóa chất tổng hợp như chất dẫn xuất của styren, thuốc nhuộm, chất chống cháy và dầu mỡ tổng hợp.
- Sản xuất polymer: Etylbenzen cũng có thể được sử dụng để sản xuất các polymer khác nhau thông qua việc chuyển đổi thành các hợp chất khác trong quá trình hóa học.
- Chất tạo màu: Etylbenzen có thể được sử dụng để sản xuất các chất tạo màu dùng trong ngành dệt nhuộm và ngành sản xuất mực in.
5. Cách phân biệt benzen, stiren, etyl benzen trong phòng thí nghiệm
Để phân biệt benzen, stiren và etylbenzen ta sử dụng thuốc thử là dung dịch KMnO4
- Mẫu thử làm mất màu của dung dịch KMnO4 ngay ở nhiệt độ thường là stiren
3C6H5-CH=CH2 + 2KMnO4 + 4H2O → 3C6H5-CH(OH)-CH2(OH) + 2MnO2 +2KOH
- 2 ống thử còn lại sẽ không có hiện tượng gì, chúng ta tiếp tục đem đun nóng 2 ống thử này. Nếu mẫu thử nào làm mất màu dung dịch KMnO4 là etylbenzen và mẫu thử không có hiện tượng gì là benzen
C6H5C2H5 + 4KMnO4 -> C6H5COOK +K2CO3+ 4MnO2+KOH+ 2H2O
Etylbenzen có ứng dụng quan trọng trong điều chế các hóa chất công nghiệp. Tuy nhiên việc tiếp xúc, sử dụng hóa chất này cần đảm bảo các yêu cầu an toàn để tránh những ảnh hưởng đến sức khỏe con người
Link nội dung: https://sgk.edu.vn/etylbenzen-h2-a69308.html